在一定环境条件下,系统发生由始态到终态的变化,称之为热力学过程,简称为过程。在不同的物理化学教材中,对于等温过程的定义存在较大的争议,因此提出了对等温过程的准确定义进行辨析的需要。
1恒温过程和等温过程的理解等温过程的定义在物理化学教材中大概有两种不同的表述:
(l)等温过程是指系统的温度维持不变且等于环境的温度的过程。
(2)等温过程是指环境温度恒定不变,系统的始终态温度相等并等于环境温度的过程。系统温度在过程中途可能发生变化,也可能不变阵4。如果在等温过程中系统的温度也恒定,则称为恒温过程。
恒温过程,顾名思义,就是无论是开始、终了还是在系统的变化过程中,系统温度都保持不变。那么等温过程呢?如果按照种定义,等温过程和恒温过程没有区别,但仔细分析,这两个过程是不同的,但在一定的条件下是等同的。如图1所不,把气缸置于恒温热源中,当活塞上的压力缓慢减小(或增加)时,缸内气体将缓慢膨胀(或压缩)而做功,同时气体与热源不断交换热量而保持温度不变,这就实现了气体的等温过程。由理想气体的状态力一程式PVNRT可知P1V1=PZV2=PVNRT恒量。在数学的角度来看,P=NRTlV这一函数式是波动曲线的拟合,也就是即使过程中温度有波动,即低于曲线,或者高于曲线,但正偏差和负偏差之和等于零,也可以近似看作等于曲线下的而积(图2)。
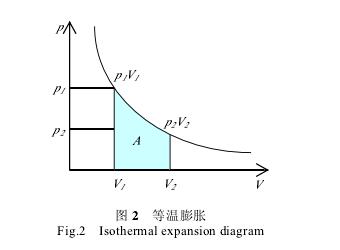
图2为等温膨胀图,其物理意义为当内外的压力只差无限小,系统内的气体缓慢做功,且无摩擦等消耗,即系统和环境能完全J灰复原状,这说明变化过程每一瞬间,系统内部都能通过外部的恒温热源进行热交换,来维持系统的温度时刻与环境的温度相等,这就是所谓的可逆过程。但是,这种可逆过程只是一种理想的过程,实际上是办不到的。
因为一个过程必定引起状态的变化,而状态的改变一定破坏平衡,也就是不能使系统的温度时刻与环境的温度相等,即存在温度的波动性。即使等温过程不是恒温过程,但当一个过程进行得非常非常慢,速度趋向于零,这样就有足够的时间使气体的压力由微小的不均匀变为均匀,同时使系统能瞬间与外部恒温热源进行热交换而保持温度不变时,此时,等温过程与恒温过程相同,或者说恒温过程就是等温可逆过程。在没有明确区分恒温过程还是等温过程的时候,必须根据上下文进行判断。如果问题中涉及缓慢等字样,或很明显过程可视为可逆过程,那么二者是一回事,系统温度维持不变并与环境温度相同。反之明显是一个快速变化的过程,就只能理解为外部热源温度恒定,而系统温度不恒定。http://www.zhpct.com